新一代基于计算病理学的TROP2生物标志物可预测datopotamab deruxtecan TROPION-Lung01 III期临床试验中非小细胞肺癌患者的临床治疗结果
2024-09-11 ichone 网络
在整体试验人群中,datopotamab deruxtecan在TROP2-QCS 生物标志物阳性的患者显示出比多西他赛显著更优的疗效。
TROPION-Lung01 III期临床试验的探索性分析结果显示,由阿斯利康专有的计算病理学平台——定量连续评分(QCS)计算的TROP2表达特征,可预测接受 datopotamab deruxtecan (Dato-DXd)治疗的晚期或转移性经治非小细胞肺癌(NSCLC)患者的临床治疗结果。在整体试验人群中,datopotamab deruxtecan在TROP2-QCS 生物标志物阳性的患者显示出比多西他赛显著更优的疗效。该结果已在国际肺癌研究协会主办的 IASLC 2024 世界肺癌大会(WCLC)的主席研讨会上发表(PL02.11)。
TROP2是一种在广泛表达于NSCLC肿瘤细胞内和膜表面的蛋白质1,2。当使用传统的基于免疫组织化学(IHC)的病理学评估时,TROP2表达无法预测患者对靶向TROP2的抗体药物偶联物(ADC)的反应3,4。QCS由阿斯利康开发,是一个由病理专家全监督的计算病理学平台,可分析患者组织样本的数字化图像并精确量化肿瘤靶点在细胞内和膜表面的表达特征,如TROP2。
Datopotamab deruxtecan是一种靶向TROP2的DXd ADC药物,由第一三共发现,阿斯利康和第一三共联合开发。
在本次分析中,QCS用于分析从TROPION-Lung01临床研究中采集到的患者组织样本,可为每个样本中的肿瘤细胞生成标准化膜比值。如果大多数(≥75%)肿瘤细胞的比值低于预定值(≤0.56),则患者的肿瘤被视为 TROP2-QCS 生物标志物阳性,这表明细胞质中TROP2 的比例相对更高。
分析显示,非鳞状NSCLC患者中TROP2-QCS 生物标志物阳性的比例高于鳞状NSCLC患者(分别为66%和44%)。生物标志物阳性临界值以不伴可靶向基因组改变的非鳞状NSCLC患者亚组的无进展生存期(PFS)做优化,因为该亚组代表了存在重大未被满足的治疗需求且无可靶向生物标志物的人群。
对于TROP2-QCS生物标志物阳性的肿瘤患者(占生物标志物可评估人群的60%,包括非鳞状和鳞状NSCLC患者),与多西他赛相比,datopotamab deruxtecan可将疾病进展或死亡风险降低43%(中位PFS 为 6.9个月 vs 4.1个月;[HR] 0.57;95% [CI] 0.41-0.79)。
而在总体试验人群的初步分析中,与多西他赛相比,datopotamab deruxtecan将疾病进展或死亡风险降低了25% (PFS为4.4个月vs 3.7个月;HR 0.75;95% CI 0.62-0.91;p=0.004),已在2023年欧洲肿瘤内科学会上公布5。
在无可靶向基因组改变且TROP2-QCS生物标志物阳性的非鳞状NSCLC患者亚组中,datopotamab deruxtecan 将疾病进展或死亡风险降低了48%(PFS为7.2个月vs 4.1个月HR 0.52;95% CI 0.35-0.78)。
芝加哥大学教授、该临床试验研究员Marina Garassino医学博士表示:“TROP2 广泛表达于实体肿瘤细胞,包括非小细胞肺癌,但它尚未被确立为任何靶向TROP2 抗体药物偶联物的预测性生物标志物。通过这项分析并借助阿斯利康的计算病理学平台,我们可以更精确地定量测量肿瘤细胞内和膜表面的TROP2,从而确定哪些非小细胞肺癌患者最有可能从datopotamab deruxtecan 治疗中获益。”
阿斯利康全球执行副总裁、肿瘤研发负责人Susan Galbraith表示:“这项分析证明了我们的计算病理学平台在发现新的预测性生物标记物和显著改善 datopotamab deruxtecan 患者筛选方面的强大功能。它还具有巨大的潜力以帮助更准确地筛选更多抗体药物偶联物产品组合的患者。我们很高兴能与罗氏诊断拓展合作,验证这种针对TROP2 的探索性方法来开发伴随诊断并尽快将其应用于临床治疗。”
第一三共全球研发负责人Ken Takeshita博士表示:“QCS分析结果支持 了TROP2(通过定量连续评分法检测)作为datopotamab deruxtecan的预测生物标志物的潜力,并能解答为什么某些非小细胞肺癌患者的治疗应答更好。这些见解对于我们进一步了解如何更准确地识别可能受益于靶向TROP2 的抗体药物偶联物的非小细胞肺癌患者至关重要。”
在生物标志物可评估人群中,未发现新的安全性信号,并且无论TROP2表达状态如何,3 级或更高级别治疗的相关不良事件(TRAE)的发生率相似。在 TROP2-QCS 生物标志物阳性患者中,datopotamab deruxtecan和多西他赛组分别有30%和46%的患者发生3级及以上级别TRAE。最常见的3级或更高级别TRAE是口腔炎(7%,3%)和眼表事件(3%,0%)。datopotamab deruxtecan和多西他赛组分别有3%和1%的患者发生了3级及以上级别的药物相关间质性肺病事件。
TROPION-Lung01 QCS 结果摘要
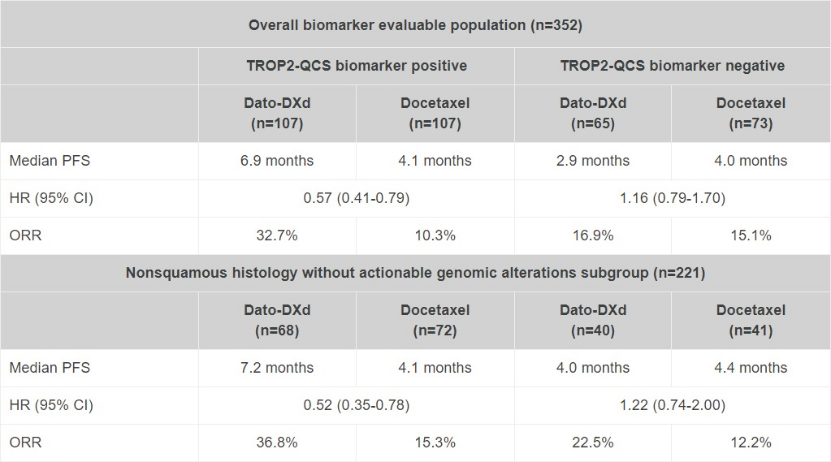
CI, 置信区间;HR,风险比;ORR,客观缓解率;PFS,无进展生存期
阿斯利康与罗氏诊断合作共同开发和商业化TROP2-QCS 生物标志物伴随诊断
阿斯利康和罗氏诊断正在扩大现有合作,共同开发一种新型伴随诊断,该诊断结合了阿斯利康专有的计算病理学平台QCS,将嵌入在罗氏的navify® 数字病理学图像管理系统中。
罗氏诊断负责人Jill German表示:“我们与阿斯利康的合作继续突破了传统肿瘤诊断的边界。通过开发超越人类能力的创新人工智能工具,该解决方案能够帮助确定哪些肿瘤患者最有可能从靶向治疗中受益,从而有可能改善患者治疗结局。”
根据此次的扩展合作,罗氏诊断和阿斯利康将基于QCS计算病理学平台,在罗氏诊断的 navify®数字病理学平台中共同开发和商业化一种新型伴随诊断,帮助病理学家确证试验性VENTANA TROP2的检测结果。
作为病理科解决方案的领先供应商,罗氏诊断提供端到端的数字病理学临床工作流程解决方案,从组织染色到生成高质量数字化图像,进而使用自动临床图像分析算法进行评估。
关于非小细胞肺癌
2022年,全球有超过250万人被诊断为NSCLC6。NSCLC是最常见的肺癌类型,约占所有肺癌分型中的80%7。其中,约75%和25%的非小细胞肺癌为非鳞状或鳞状组织学8。虽然免疫疗法和靶向疗法改善了转移性肺癌在一线治疗后的预后,但大多数患者最终会出现疾病进展并接受化疗治疗9-11。数十年来,尽管疗效有限且存在明显的副作用,在没有其他治疗方案的情况下,化疗一直是晚期NSCLC患者的最后治疗手段9-11。
TROP2是一种在绝大多数肺癌中高度表达的蛋白质1。目前尚无针对靶向TROP2的ADC被批准用于治疗肺癌患者12-13.
关于TROPION-Lung01临床试验
TROPION-Lung01是一项全球性、随机、多中心、开放标签的III期研究,旨在评估datopotamab deruxtecan(6.0 mg/kg)与多西他赛(75 mg/m2)在局部晚期或转移性NSCLC且接受过至少一种既往治疗的有/无可靶向基因组改变的人群的疗效和安全性;无已知的可靶向基因组改变的患者既往接受过同步或序贯铂类化疗和 PD-1 或 PD-L1 免疫治疗。具有可靶向基因组改变的患者之前接受过铂类化疗和已获批的靶向药物。
TROPION-Lung01 的双重主要研究终点是通过盲法独立中心审查 (BICR) 评估的PFS和 OS。 关键次要终点包括研究者评估的 PFS、客观缓解率、缓解持续时间、缓解时间和由BICR和研究者评估疾病控制率以及安全性。
TROPION-Lung01 在亚洲、欧洲和南美洲地区招募了约600名患者,更多信息请访问ClinicalTrials.gov。
关于Datopotamab deruxtecan
datopotamab deruxtecan是一种处于研究阶段的靶向TROP2的ADC。datopotamab deruxtecan 采用第一三共专有的 DXd ADC 技术设计,是第一三共肿瘤产品线中的六个领先ADC 之一,也是阿斯利康 ADC科学平台中最先进的项目之一。datopotamab deruxtecan 由与札幌医科大学合作开发的人源化抗 TROP2 IgG1 单克隆抗体组成,通过基于四肽的可裂解连接子与一组拓扑异构酶 I 抑制剂有效载荷(一种 exatecan 衍生物)相连。
datopotamab deruxtecan的全球综合开发计划正在进行中,有 20多项临床试验评估其在非小细胞肺癌、三阴性乳腺癌、激素受体阳性/ HER2阴性乳腺癌等多种实体瘤中的疗效和安全性。该计划包括七项肺癌III期临床试验和五项乳腺癌III期临床试验,评估 datopotamab deruxtecan作为单药以及与其他疗法的联合使用。
参考文献
1. Mito R, et al. Clinical impact of TROP2 in non‐small lung cancers and its correlation with abnormal p53 nuclear accumulation. Pathol Int. 2020;70(5):287-294.
2. Shvartsur A, et al. Trop2 and its overexpression in cancers: regulation and clinical/therapeutic implications. Genes & Cancer. 2015 Mar;6(3-4): 84-105.
3. Shimizu T, et al. J Clin Oncol 2023;41:4678-87.
4. Heist RS, et al. J Clin Oncol. 2017;35:2790-7.
5. Ahn M-J, et al. Datopotamab deruxtecan (Dato-DXd) vs doxetaxel in previously treated advanced/metastatic (adv/met) non-small cell lung cancer (NSCLC): results of the randomized phase 3 study TROPION-Lung01. Presented at: ESMO Congress 2023, 20-24 October 2023; Madrid, Spain. LBA12.
6. World Health Organization. Global Cancer Observatory: Lung. Available at: https://gco.iarc.who.int/media/globocan/factsheets/cancers/15-trachea-bronchus-and-lung-fact-sheet.pdf. Accessed September 2024.
7. Cancer.net. Lung Cancer – Non-Small Cell: Statistics. Available at: https://www.cancer.net/cancer-types/lung-cancer-non-small-cell/statistics#:~:text=NSCLC%20is%20the%20most%20common,be%20diagnosed%20with%20lung%20cancer. Accessed September 2024.
8. National Cancer Institute. SEER Cancer Statistics Factsheets: Lung and Bronchus Cancer, 1975-2017. Accessed September 2024.
9. Chen R, et al. Emerging therapeutic agents for advanced non-small cell lung cancer. J Hematol Oncol. 2020;13(1):58.
10. Majeed U, et al. Targeted therapy in advanced non-small cell lung cancer: current advances and future trends. J Hematol Oncol. 2021;14(1):108.
11. Pircher, A, et al. Docetaxel in the Treatment of Non-small Cell Lung Cancer (NSCLC) – An Observational Study Focusing on Symptom Improvement. Anticancer Research. 2013;33(9):3831-3836.
12. Rodríguez-Abreau D, et al. Pemetrexed plus platinum with or without pembrolizumab in patients with previously untreated metastatic nonsquamous NSCLC: protocol-specified final analysis from KEYNOTE-189. Ann Onc. 2021 Jul;32(7): 881-895.
13. American Cancer Society. Targeted Drug Therapy for Non-Small Cell Lung Cancer. Available at: https://www.cancer.org/cancer/types/lung-cancer/treating-non-small-cell/targeted-therapies.html. Accessed September 2024.
作者:ichone
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









#非小细胞肺癌#
6