Xtandi成**获批FDA 前列腺癌口服疗法
2019-12-17 佚名 药明康德
今日,安斯泰来(Astellas)和辉瑞(Pfizer)公司宣布,美国FDA批准Xtandi(enzalutamide)扩展适应症,治疗转移性激素敏感性前列腺癌(mHSPC)患者。新闻稿指出,这一批准,让Xtandi成为首款获得FDA批准,治疗三种不同形态晚期前列腺癌(非转移性和转移性去势抵抗性前列腺癌,和转移性去势敏感性前列腺癌)的口服疗法。
今日,安斯泰来(Astellas)和辉瑞(Pfizer)公司宣布,美国FDA批准Xtandi(enzalutamide)扩展适应症,治疗转移性激素敏感性前列腺癌(mHSPC)患者。新闻稿指出,这一批准,让Xtandi成为首款获得FDA批准,治疗三种不同形态晚期前列腺癌(非转移性和转移性去势抵抗性前列腺癌,和转移性去势敏感性前列腺癌)的口服疗法。
前列腺癌是全球男性中第二常见的癌症。而转移性激素敏感性前列腺癌意味着患者的癌症已经从前列腺扩散到身体的其它部位,不过这些患者的肿瘤仍然能对降低雄激素水平的治疗方法产生反应。据统计,在美国,2019年有大约4万人患有mHSPC。
Xtandi是一种特异性雄激素受体抑制剂,它不但能够阻断雄激素与受体的结合,而且能够抑制受体向细胞核内转移,以及雄激素受体与DNA的结合。因此它不仅仅是雄激素受体的拮抗剂,对雄激素信号通路也有抑制作用。
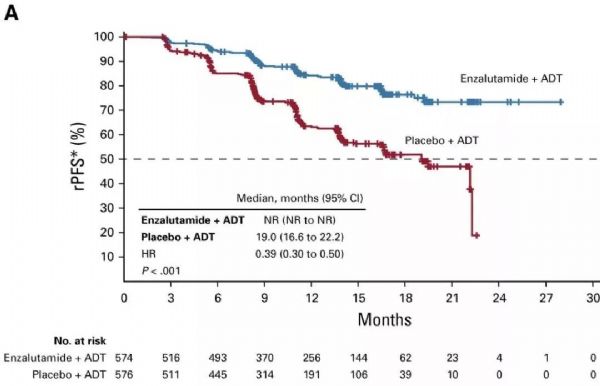
名为ARCHES的3期临床试验结果表明,与安慰剂和雄激素剥夺疗法(ADT)联用相比,Xtandi与ADT联用将患者出现放射学进展或死亡的风险降低61%(HR=0.39, 95% CI:0.30-0.50,p<0.0001)。同时,Xtandi+ADT治疗组中更多患者的前列腺特异性抗原(PSA)降低到无法检测到的水平(p<0.001)。这一试验结果已经在Journal of Clinical Oncology上发表。
ARCHES临床试验数据
“自从在2012年首次获批,Xtandi已经成为治疗去势抵抗性前列腺癌患者的标准疗法,用于治疗世界上超过42万名患者,”安斯泰来公司高级副总裁兼肿瘤学治疗领域负责人Andrew Krivoshik博士说:“这一批准让Xtandi能够在更早阶段治疗晚期前列腺癌患者。”
作者:佚名
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言
小提示:本篇资讯需要登录阅读,点击跳转登录







#Xtandi#
30
前列腺癌相关研究,学习了,谢谢梅斯
36