NEJM:全基因组测序 vs细胞遗传学检测在髓系肿瘤患者风险分层中的应用
2021-03-11 MedSci原创 MedSci原创
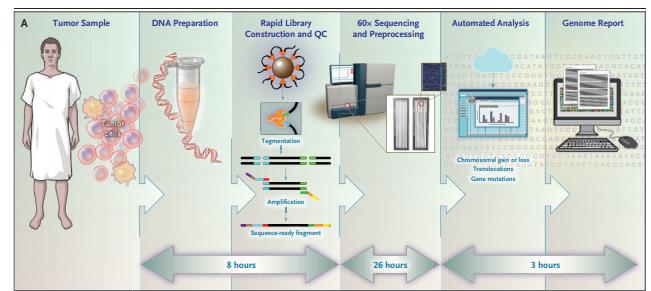
全基因组测序可以为AML或MDS患者提供快速准确的基因组图谱,其诊断效率优于传统的细胞遗传学分析,对患者的风险分层更为准确。
基因图谱在肿瘤诊断、临床结果预测和对靶向治疗应答预测方面发挥了越来越重要的作用。临床上任何个体类型肿瘤突变通常跨越广泛的基因组事件,包括染色体重排、基因扩增和缺失以及单核苷酸变化。基因图谱分析对急性髓系白血病(AML)或骨髓增生异常综合征(MDS)患者的风险分层至关重要,通常采用细胞遗传学分析。 全基因组测序是传统细胞遗传学和测序方法的潜在替代手段,近日研究人员考察了全基因组测序在髓系肿瘤患者风险分层中的应用。 研究人员使用简化的全基因组测序方法获得263例髓系肿瘤患者的基因组图谱,其中235例患者事先进行了细胞遗传学分析。研究人员采用欧洲白血病网络(ELN)指南对样本制备、测序和分析进行调整,以检测风险突变,并尽量减少周转时间。通过将全基因组测序结果与细胞遗传学分析和靶向测序后的结果进行比较,考察了全基因组测序的性能。 全基因组测序检测到所有通过细胞遗传学分析鉴定的突变,包括40个频发易位和91个拷贝数改变。此外,在235名患者中,40名(17.0%)报告了新的临床风险基因组事件。对117名患者样本进行前瞻性测序,中位数为5天,29名患者(24.8%)提供了新的基因信息
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







#遗传学#
53
#遗传学检测#
59
#髓系肿瘤#
62
#细胞遗传#
53
#全基因组测序#
55