FDA接受Tralokinumab治疗中重度特应性皮炎的BLA
2020-07-10 Allan MedSci原创
Tralokinumab治疗中度至重度特应性皮炎的生物制剂许可申请(BLA)已获美国FDA的批准。
特应性皮炎(AD)是一种慢性、瘙痒性、炎症性皮肤病,最常累及儿童,但也累及许多成人。特应性皮炎的临床特征包括皮肤干燥、红斑、渗出和结痂,以及苔癣样变。瘙痒是此病的标志,并且是给患者及其家人造成疾病负担的主要原因。
专注于皮肤病的制药公司LEO Pharma今日宣布,Tralokinumab治疗中度至重度特应性皮炎的生物制剂许可申请(BLA)已获美国FDA的批准。Tralokinumab是一种全人源单克隆抗体,可特异性中和白细胞介素13(IL-13),IL-13是特应性皮炎的关键驱动因子。关键III期临床试验(ECZTRA 1、2、3研究)已证实tralokinumab的安全性和有效性。
LEO Pharma副总裁Kim Kjølle博士说:“对于无法控制的中重度特应性皮炎患者,医疗需求仍未得到满足。如果Tralokinumab获得批准,Tralokinumab可能成为第一个可特异性中和IL-13的生物制剂”。
欧洲药品管理局(EMA)最近接受了tralokinumab的销售许可申请(MAA),并且人用药品委员会(CHMP)正在进行法规审查。

原始出处:
作者:Allan
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言













#mAb#
44
#TRA#
57
#tralokinumab#
63
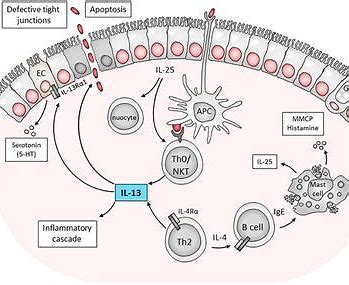
IL-13是特应性皮炎的关键驱动因子
105