JCO | PACE试验:氟维司群+帕博西尼+阿维鲁单抗(F+P+A)方案在CDK4/6抑制剂进展后激素受体阳性/HER2阴性转移性乳腺癌患者中具有较好的疗效和安全性
2024-04-05 daikun MedSci原创
评估了在一线CDK4/6抑制剂和内分泌治疗进展后,继续使用CDK4/6抑制剂是否有益,以及添加免疫检查点抑制剂是否能提高疗效,研究结果显示氟维司群+帕博西尼+阿维鲁单抗的方案具有较好的疗效和安全性。
激素受体阳性/人表皮生长因子受体2阴性晚期乳腺癌约占所有晚期乳腺癌的60%,内分泌治疗是主要的治疗手段,目前CDK4/6抑制剂与内分泌治疗联合使用,已被证实能显著改善激素受体阳性晚期乳腺癌患者的无进展生存期,近期发表在《Journal of clinical oncology》上的一项研究评估了在一线CDK4/6抑制剂和内分泌治疗进展后,继续使用CDK4/6抑制剂是否有益,以及添加免疫检查点抑制剂是否能提高疗效。

方法
入选的受试者必须为激素受体阳性/HER2阴性转移性乳腺癌患者,并且已经对CDK4/6抑制剂和芳香化酶抑制剂治疗进展,该研究将受试者(220名)按照1:2:1的比例随机分为3组,分别接受氟维司群(F)(55名)、氟维司群加帕博西尼(F+P)(111名)以及氟维司群加帕博西尼和阿维鲁单抗(F+P+A)(54名)治疗,所有治疗以28天为一个周期,主要终点为研究者评估的无进展生存期(PFS)。
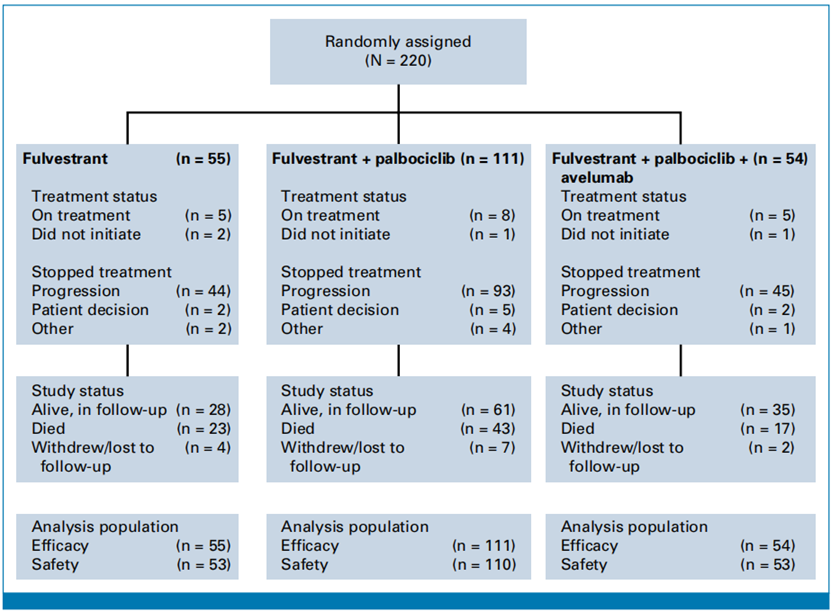
研究结果
无进展生存期(PFS):F组的中位PFS为4.8个月,F+P组的中位PFS为4.6个月(HR vs F, 1.11, 90% CI 0.79-1.55, P=0.62),F+P+A组的中位PFS为8.1个月(HR vs F, 0.75, 90% CI 0.50-1.12, P=0.23)。客观反应率(ORR):F组为7.3%,F+P组为9.0%,F+P+A组为13.0%。临床获益率:F组为29.1%,F+P组为32.4%,F+P+A组为35.2%。总体生存期(OS):F组的中位OS为27.5个月,F+P组的中位OS为24.6个月(HR vs F, 1.02, 90% CI 0.67-1.56),F+P+A组的中位OS为42.5个月(HR vs F, 0.68, 90% CI 0.40-1.15)。探索性分析:在ESR1突变患者中,F+P组的中位PFS显著长于F组。在PIK3CA突变患者中,F+P组的中位PFS显著长于F组。

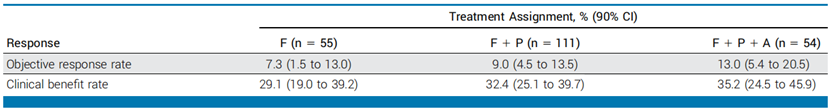
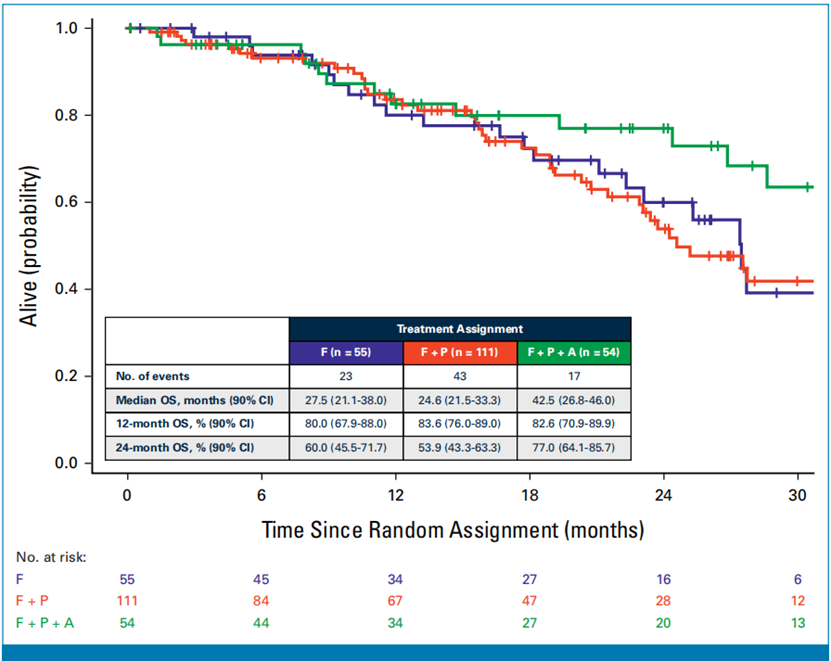
安全性
共有216例患者开始治疗,其中84例(38.9%)发生3/4级治疗相关不良反应。F组:仅有1例(1.9%)发生3/4级不良反应,最常见的不良反应为乏力(34.0%),F+P组:46例(41.8%)发生3/4级不良反应,最常见的不良反应为中性粒细胞减少(65.5%,32.7%为3/4级)、乏力(34.5%)和贫血(21.8%),F+P+A组:37例(69.8%)发生3/4级不良反应,最常见的不良反应为中性粒细胞减少(73.6%,49.1%为3/4级)、乏力(64.2%)、贫血(34.0%)和血小板减少(32.1%),免疫相关不良反应:F+P+A组中52.8%的患者出现潜在的免疫相关不良反应,最常见的是AST升高(11.3%)和ALT升高(9.4%),3/4级免疫相关不良反应较少见,剂量调整:F+P组和F+P+A组分别有40例(36.0%)和31例(57.4%)需要因毒性而暂停帕博西尼治疗,25例(22.5%)和11例(20.4%)需要降低帕博西尼剂量,21例(38.9%)需要因毒性而暂停阿维鲁单抗治疗,综上所述,F+P+A组的不良反应发生率最高,主要表现为血液学毒性,这表明该方案的安全性较好,但在临床应用中需要密切监测和处理不良反应。

结论
对于激素受体阳性/HER2阴性转移性乳腺癌患者,在CDK4/6抑制剂和芳香化酶抑制剂治疗进展后,继续使用帕博西尼并切换内分泌治疗到氟维司群并不能显著提高PFS,与氟维司群单药治疗相比(中位PFS 4.8个月 vs 4.6个月,HR 1.11,P=0.62)。然而在氟维司群、帕博西尼的基础上加用阿维鲁单抗可显著提高PFS,与氟维司群单药治疗相比(中位PFS 8.1个月,HR 0.75,P=0.23)。安全性方面,F+P+A组的3/4级不良反应发生率最高,主要表现为血液学毒性。这些结果表明,F+P+A方案在CDK4/6抑制剂进展后激素受体阳性/HER2阴性转移性乳腺癌患者中具有较好的疗效和安全性,值得进一步研究。
原始出处
Erica L. Mayer et al.,PACE: A Randomized Phase II Study of Fulvestrant, Palbociclib, and Avelumab After Progression on Cyclin-Dependent Kinase 4/6 Inhibitor and Aromatase Inhibitor for Hormone Receptor–Positive/Human Epidermal Growth Factor Receptor–Negative Metastatic Breast Cancer. JCO 0, JCO.23.01940.DOI:10.1200/JCO.23.01940.
作者:daikun
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#乳腺癌# #氟维司群# #CDK4/6抑制剂# #帕博西尼#
17